tehnik esterifikasi etil asetat dari Etanol.
A. PELAKSANAAN PRAKTIKUM
1· Tujuan Praktikum :
a. Mempelajari tehnik esterifikasi etil asetat dari Etanol.
b. Mempelajari mekanisme reaksi esterifikasi etil asetat dan etanol.
B. LANDASAN TEORI
Ester dapat dibuat dari asam dan alcohol atau dari anhidrida asam dan alcohol. Esterifikasi atau pembuatan ester terjadi jika asam karboksilat dipanaskan bersama alcohol primer atau sekunder dengan sedikit asam mineral sebagai katalis. Metil salisilat, yang juga disebut minyak gandapura digunakan untuk membentuk cita rasa dan dalam obat gosok untuk mengurangi nyeri otot. Beberapa cara digunakan untuk mengganggu kesetimbangan reaksi tersebut agar hasil produksinya meningkat. Reaksi esterifiksi dapat digeser kearah reaksi sempurna jika digunakan salah satu pereaksi (asam atau alcohol) secara berlebihan, atau air yang terbentuk dibuang dari campuran reaksi. produksi ester secara industry dilakukan dengan mereaksikan anhidrida asam dengan alcohol ( Antony. 1992: 149-150).
Monosakarida mengandung beberapa gugus hidroksil. Tidak mengherankan jika monosakarida menjalani reaksi-reaksi alcohol. Misalnya ia dapat diubah menjadi ester melalui reaksi dengan turunan asam, misalnya perubahan β-D-glikosa menjadi penta asetat dengan asam anhidrida. Hidroksil hemiasetal pada C-1 serta semua hidroksilnya teresterifikasi (Hart. 1990: 344).
Alkil ester yang tidak dihalangi dapat dibuat melalui esterifikasi sederhana dengan memanaskan suatu asam karboksilat dengan suatu alcohol dan sedikit asam kuat. Ester estrik terhalangi dan fenil ester tidak dapat dibuang dengan esterifikasi sederhana. Ester-ester ini seperti ester alkil yang tidak terhalangi dapat dibuat dari reaksi karboksilat yang reaktif – suatu asam halide atau anhidrida dengan suatu alcohol atau fenol. Hiidrolisis dari suatu ester menghasilkan asam karboksilat dan alcohol. Reaksi ini adalah reaksi kebalikan dari esterifikasi langsung suatu asam karboksilat dan alcohol. Untuk mandorong reakksi ke arah pembentukn ester digunakan asam karboksilat atau alcohol berlebih menghasilkan air. Untuk hidrolisis dalam suasana asam kita gunakan air yang sangat berlebihan untuk mendorong kesetimbangan kea rah karboksilat – alcohol ( Fessenden. 2009: 481-482).
C. ALAT DAN BAHAN PRAKTIKUM
1. ALAT PRAKTIKUM
· Labu alas bindar 500 ml
· Corong pisah
· Pipet tetes
· Pipet volum 25 ml
· Pipet gondok (25 ml, 10 ml)
· Alat refluk
· Alat destilasi
· Erlenmeyer
· Gelas ukur
· Neraca analitik
· Stopwach
· Thermometer
2. BAHAN PRAKTIKUM
· Larutan etanol
· Larutan H2SO4 pekat
· Asam asetat glacial
· Aquades
· Larutan NaHCO3 jenuh
· MgSO4 anhidrat
· Kertas saring
D. SKEMA KERJA
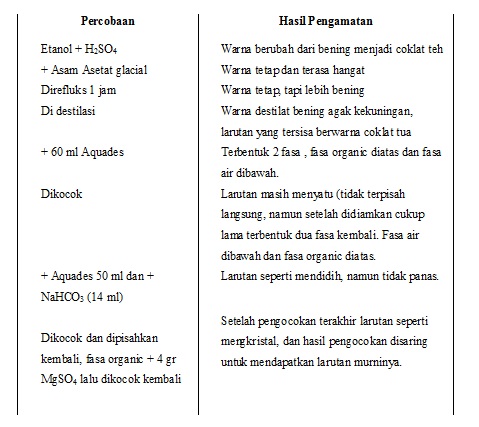
E. HASIL PENGAMATAN
F. ANALISIS DATA
1) Persamaan Reaksi
H3C-COOH + HO-CH2-CH3 → H3C-COO-CH2-CH3 + H2O
2) Mekanisme Reaksi
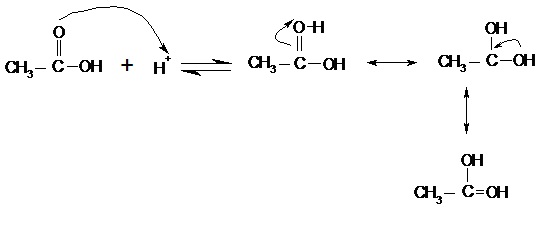
a. Protonasi gugus karbonil
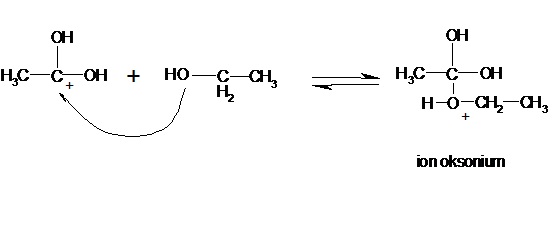
b. Adisi gugus nukleofil
c. Pelepasan H+ dan protonasi oksigen
d. Pelepasan molekul air dan H+
G. PEMBAHASAN
Pada praktikum kali ini mempelajari teknik esterifikasi etil asetat dari etanol serta mempelajari mekanisme reaksi esterifikasi etil asetat dari etanol. Ester dapat dibuat dari asam dan alkohol atau dari anhidrida asam dan alkohol dimana esterifiakasi atau pembuatan ester terjadi jika asam karboksilat dipanaskan bersama alkohol primer atau sekunder dengan sedikit asam mineral sebagai katalis. Dalam hal ini esterifikasi yang dibuat dari etanol.
Jika asam karboksiklat dipanaskan dengan alkohol dengan katalis asam(H2SO4 atu HCl) terdapat kesetimbangan antara ester dan air:
Proses ini disebut dengan esterifikasi.
Pada praktikum kali ini,dalam pembuatan ester digunakan asam asetat glasial,etanol absolut serta H2SO4 sebagai katalis.Pada praktikum ini,penambahan H2SO4 dilakukan secara pelahan-lahan.Hal ini dimaksudkan agar tidak terjadi letupan-letupan,karena reaksi ini bersifat eksoterm. Reaksi estrifikasi bersifat reversibel,sehingga untuk memproleh rendemen yang tinggi dari ester itu,kesetimbangan harus digeser kearah ester itu sendiri (Fessenden,2010).Untuk menggeser ketimbangan reaksinya,pada praktikum ini dilakukan metode refluks untuk memaksimalkan reaksi.Refluks adalah suatu pemanasan berulang yang dimaksudkan untuk menyepurnakan reaksi sehingga reaksi berjalan kearah produk,dimana terjadi proses kondensasi yang dapat meningkatkan energi kinetik dengan danya tumbukan antar partikel (Anonim,2007).Pada praktikum ini refluks dilakukan kuarang lebih selam 1 jam dengan penangas air,karena suhu refluks dibawah titik didih air,yaitu 70⁰C.Setelah itu proses selanjutnya dilakukan destilasi.Destialsi adalah salah satu cara ntuk mengisolasi suatu senyawa oraganik yang terdapat pada suatu campuaran dari dua larutan titik.Umumnya destilasi menyangkut pemisahan cairan diman perbedaan tekanan uap diambil sebagai keuntungan untuk memisahkan materi tersebut(Debbig,1987). Setelah dilakukan destilasi didapat destilatnya,ester menguap pada suhu 70⁰C. Kemudian destilatnya diekstraksi dengan aquadest dan NaHCO3,penambahan ini bertujuan untuk mengikat pengotor yang ada dalam destilatnya,karena pada destilat itu,bukan ester murni. Pada proses ekstraksi,lapisan ester berada diatas yang berwarna bening,dan berwarna putih keruh adalah fasa air. Setelah dipisahakan fasa esternya,ditambahkan Na2SO4 anhidrat,yang tujuanya untuk menyerap molekul H20 yang mungkin terbawa pada waktu pemisahan dengan corong pisah. Namun dalam praktikum ini,ester yang didapat sedikit sehingga sangat sulit dihitung persen yang didapat. Namun hanya bisa di amati ester,cairan berwarna bening dan berbau khas dan muadah menguap.
H. KESIMPULAN
· Ester dapat dibuat dengan asam asetat glasial,etanol absolut dengan katalis H2SO4 pekat dengan metode refluks dan destilasi yang dilanjutkan dengan ekstraksi pada destilatnya.
· Pemurnian ester dapat dilakukan dengan menambahakan NaHCO3 dan Na2SO4 anhidrat.
· Ester yang didapat dengan bahan ini adalah etil asetat yang berwarna bening dan berbau khas serta mudah menguap.
DAFTAR PUSTAKA
Anonim.2007.Esterificotion diacces dari: http://en.gop.au/database/subtance info/profile/38.html. pada tanggal 25 april 2010 pukul :19.30 wita.
Fassenden.D.D.1897.General Chemistry 2th edition,Massachusetts:Hougthon Miffin Company.
Hart.Harlod.2003.Kimia Organik.Jakarta : Erlangga.
Keenan,dkk.1992.Ilmu Kimia Untuk Universitas Jilid 2.Jakarta:Erlangga.
Wilbrahan,A.Cdan Michael Matta.1992.Pengantar Kimia Organik dan Hayati. Bandung :ITB